Vom aborda astăzi o serie de fenomene din domeniul comun al căldurii, presiunii şi dilatării corpurilor. Căci veţi vedea, că tocmai prin studierea interdependenţei unor asemenea fenomene ni se va deschide drumul pentru înţelegerea a ceea ce este de fapt fiinţa/natura căldurii. Vom analiza mai întâi fenomenul ce se revelează prin conţinutul acestor trei tuburi (Vezi 1, 2, 3 în Fig. 6.1).
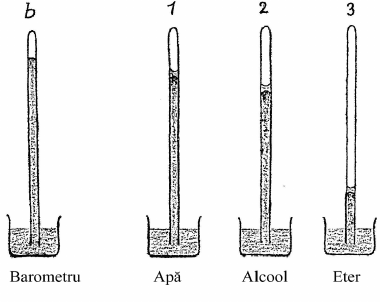
În primul tub din dreapta (1) avem o coloană de mercur, ca într-un tub barometric obişnuit, iar deasupra mercurului este puţină apă. Apa, aflându-se într-un astfel de spaţiu, se evaporă continuu. Avem apă în aşa-numitul vacuum, în spaţiul gol, şi putem spune că apa se evaporă. Cantitatea mică de apă ce este în interior se evaporă continuu. Putem constata această evaporare prin prezenţa vaporilor de apă ce se află acolo: Dacă se compară înălţimea coloanelor de mercur, observăm că coloana de mercur din tubul (1) se află mai jos decât coloana de mercur de aici (b); aceasta din cauză că în tubul (1) există vapori de apă, care creează o presiune ce acţionează de sus, pe când în coloana de mercur (b) nu există nicio presiune de nicăieri, ea aflându-se la presiunea normală a aerului, deasupra ei neexistând apă evaporată, deci nici vapori de apă. Acolo este un spaţiu gol, astfel că doar această coloană de mercur ţine echilibrul presiunii atmosferice. Dacă măsurăm, constatăm că în (1) coloana de mercur este mai mică decât coloana de mercur de aici din (b), datorită presiunii exercitată de aşa-numita tensiune a apei evaporate. Vedem deci că aburul apasă întotdeauna pe pereţi şi exercită o anumită presiune conform unei anumite stări calorice. Acest lucru îl putem constata dacă încălzim partea superioară a tuburilor. Veţi vedea, că dacă temperatura creşte, coloana de mercur va coborî, ceea ce înseamnă că presiunea devine mai mare. Vom vedea deci, că aburul apasă pereţii cu atât mai mult, cu cât temperatura lui creşte. Observaţi cum coloana de mercur deja coboară şi cum tensiunea interioară, forţa de apăsare, creşte cu temperatura. Volumul pe care aburul vrea să-l ocupe se măreşte.
În tubul al doilea (2) avem alcool deasupra mercurului. Îl vedeţi şi aici ocupând – ca lichid – un anumit spaţiu. Şi el se evaporă, coborând şi mai mult coloana de mercur faţă de cea a barometrului din stânga. Dacă măsor, voi constata însă că coloana de mercur este şi mai coborâtă decât în cazul coloanei ce se afla sub influenţa apei evaporate. Trebuie să aşteptăm aici (1) până ce coloana va urca din nou, revenind la poziţia de dinaintea încălzirii. Vom descoperi cu această ocazie, că tensi unea depinde de asemenea de substanţa însăşi pe care o folosim. Deci tensiunea care ia naştere este mai mare la alcool decât la apă. Şi aici – în (2) – putem încălzi. Veţi vedea, că tensiunea este mult mai mare decât cea a apei, dacă mărim temperatura. Dacă răcim aburul până la temperatura iniţială, mercurul urcă datorită presiunii mai mici, a tensiunii interne mai mici. Vedeţi cum coloana urcă.
În tubul al treilea (3) am pus – exact în aceleaşi condiţii – eter, care la rândul său se evaporă. Vedeţi că aici coloana este foarte coborâtă. Din aceasta rezultă, că dacă volatilizăm eterul în aceleaşi condiţii, el presează substanţial diferit faţă de apa evaporată. Prin urmare, presiunea exercitată de un gaz asupra ambianţei depinde de temperatură, dar şi de substanţa respectivă. Şi aici puteţi observa, că prin încălzire volumul se măreşte mult mai mult, că deci eterul evaporat apăsă cu mult mai puternic. Continuăm să ne menţinem şi aici în domeniul fenomenelor, deoarece vrem să ajungem la un rezultat tocmai prin această privire de ansamblu asupra lor.
Iar acum ţin în mod special să vă prezint următorul fenomen: Cunoaşteţi din consideraţiile anterioare, ca şi din fizica elementară, că putem transforma corpurile solide în lichide, pe cele lichide în solide, atunci când le trecem în sus şi în jos prin aşa-numitul punct de topire. Dacă un corp lichid devine din nou solid, adică este coborât sub punctul de topire, atunci ne apare ca un corp solid. Lucrul curios, pe care trebuie să-l avem din nou în vedere în cadrul privirii noastre de ansamblu, este că dacă la corpul solid aplicăm o presiune mai mare decât cea la care el s-a solidificat, el poate redeveni lichid. Deci el poate fi adus în stare lichidă la o temperatură mai mică decât cea de solidificare. Ştiţi că la 0°C apa trece în stare solidă, devine gheaţă. Deci gheaţa ar trebui să fie un corp solid la toate temperaturile aflate sub 0°C. Vom face acum cu această gheaţă un experiment, prin care veţi vedea că ea poate fi adusă în stare fluidă fără să mărim temperatura. În condiţii normale, dacă vrem să o aducem la starea lichidă, trebuie să ridicăm temperatura, dar noi nu vom ridica temperatura, ci vom exercita asupra gheţii o presiune foarte mare. Presiunea o exercităm prin faptul că atârnăm această greutate [Nota 24]. Aici gheaţa se va topi. Veţi vedea deci că gheaţa este secţionată, deoarece local devine lichidă sub acţiunea presiunii exercitate de sârmă. Vă veţi aştepta ca acest bloc de gheaţă să cadă jos în două bucăţi, una în dreapta şi una în stânga, deoarece la mijloc el devine lichid. Dacă am face experimentul mai repede, l-am vedea până la capăt. (Străbaterea blocului de gheaţă de către sârmă decurge aşa de încet, încât abia la sfârşitul orei s-au spus cele ce urmează:) Dacă priviţi acum aici, veţi vedea cum chiar dacă aţi fi aşteptat până ce secţionarea ar fi fost terminată, nu aţi fi avut de ce să vă temeţi, că gheaţa ar cădea şi s-ar rupe în două bucăţi. Gheaţa se reface imediat la loc deasupra sârmei, care trece de sus în jos, iar blocul de gheaţă rămâne întreg. Din aceasta vedeţi, că acolo unde se exercită presiunea prin intermediul sârmei se formează lichid. Dar în clipa în care nu se mai exercită presiune, lichidul se solidifică imediat, devenind iar gheaţă, adică ea se reface, reunindu-se. Această fluidificare a gheţii lcontinuă doar sub influenţa presiunii respective, dacă temperatura rămâne constantă. Deci şi un corp solid poate fi fluidificat sub punctul său de topire. Dar pentru ca starea să persiste, este necesară continuarea acţiunii presiunii. Dacă presiunea încetează, reapare starea solidă. Acest lucru l-aţi constata, dacă am aştepta câteva ore.
Al treilea aspect pe care trebuie să-l studiem, şi care va constitui un sprijin în plus pentru consideraţiile noastre, este următorul: Am putea să luăm diverse substanţe, căci în principiu, ceea ce vrem să arătăm este de fapt valabil pentru toate acele substanţe ce pot forma împreună un aliaj, adică se pot uni în aşa fel, încât se întrepătrund reciproc fără a face reacţii chimice de legătură. Avem aici plumb într-un creuzet. Plumbul este o substanţă ce se topeşte, adică trece de la starea solidă la cea lichidă la 327°C. Într-un alt creuzet avem Bismut, care se topeşte la 269°C, iar aici avem zinc, care se topeşte la 232°C. Avem deci trei corpuri cu punctul de topire peste 200°C. Vom uni aceste trei corpuri, topindu-le mai întâi, într-un aliaj, adică trecându-le în stare lichidă, astfel încât ele se întrepătrund reciproc fără să realizeze o legătură chimică (cele trei metale sunt topite separat şi apoi turnate împreună). Vă puteţi uşor imagina, că dacă introducem în apă clocotită pe oricare din aceste trei metale cu punctul de topire peste 200°C, el se va solidifica, deoarece apa îşi are la 0°C punctul de topire şi la 100°C pe cel de fierbere; prin urmare niciunul dintre aceste trei metale nu va putea ajunge la topire în această apă. O să facem acum experimentul de a introduce aliajul, întrepătrunderea celor trei metale, în apa care fierbe. Putem constata de pe acum ce se întâmplă de fapt. Ţinem termometrul în interiorul aliajului celor trei metale şi stabilim fix o temperatură de 175°C a amestecului metalic, care încă este în stare fluidă. Ştiţi că nici unul dintre metalele individuale nu ar mai fi lichid la această temperatură, ci ar fi deja solid. Aliajul celor trei metale este încă lichid. Puteţi deduce de aici, că dacă amestecăm diverse metale poate apărea fenomenul, că punctul de topire – punctul la care amestecul metalic devine fluid –, este mai coborât decât punctul de topire al fiecărui metal în parte. Vedeţi prin urmare, că corpurile se influenţează reciproc. Şi tocmai prin acest fenomen noi putem crea o bază importantă pentru privirea de ansamblu asupra fenomenelor calorice.
Turnăm cu grijă aliajul metalic, aflat încă în stare lichidă la 100°C, în apa clocotindă, ce are tot 100°C. Să lăsăm acum apa să se răcească. Să observăm temperatura. Aliajul metalic este încă lichid, apoi va deveni solid. Aceasta înseamnă, că ajungem sub punctul de topire, iar în timp ce apa se răceşte sub punctul de fierbere putem constata – după temperatura apei în acel moment –, când se solidifică aliajul metalic, deci unde este punctul său de topire. Prin urmare, vedeţi că punctul de topire al amestecului este mai scăzut [Nota 25] decât punctul de topire al fiecărui metal în parte.
Am adus aceste fenomene în completarea celorlalte, tocmai pentru a obţine o privire de ansamblu mai cuprinzătoare, iar acum putem adăuga alte câteva consideraţii la cele expuse ieri privitor la deosebirea dintre stările solidă, lichidă şi gazoasă sau de vapori. După cum ştiţi, corpurile solide, în special un număr mai mare de metale şi alte minerale, apar nu într-o formă nedefinită, ci în forme foarte bine definite [Nota 26], în aşa-numitele cristale. Astfel, că putem spune: În condiţiile obişnuite în care trăim noi pe Pământ, corpurile solide ne întâmpină sub formă de cristale, deci în forme foarte bine determinate. Fireşte că aceasta ne face atenţi, să reflectăm asupra modului în care iau naştere asemenea forme cristaline, ce forţe stau la baza acestor forme de cristale. Pentru a dobândi reprezentări privitoare la aceste lucruri, va trebui să vedem cum se comportă întreaga sumă a corpurilor solide aflate pe suprafaţa Pământului, care nu sunt legate direct de masa acestuia. Vă este cunoscut faptul, că dacă ţinem în mână un corp solid oarecare şi-l lăsăm liber, el cade pe Pământ. Acest lucru este indicat de obicei în fizică spunându-se, că Pământul atrage aceste corpuri solide, că el exercită o forţă. Corpul cade pe Pământ sub influenţa acestei forţe a gravitaţiei.
Dacă avem o masă lichidă oarecare şi apoi o răcim, ea poate să capete, când devine solidă, chiar şi o anumită formă cristalină. Acum se naşte întrebarea: Care este de fapt relaţia dintre acea forţă, forţa de gravitaţie, căreia i se supun mai întâi toate corpurile solide, şi forţele, care trebuie să existe şi ele la rândul lor, care trebuie să acţioneze într-un anumit mod pentru ca corpurile solide să ia forme cristaline? Este firesc să gândiţi, că forţa de gravitaţie ca atare, prin care un corp cade pe Pământ – dacă este să vorbim despre o asemenea forţă de gravitaţie –, nu poate fi ceva, care să aibă în acelaşi timp de-a face cu alcătuirea formelor cristalelor. Căci acestei forţe de gravitaţie i se supun toate formele de cristale; oricum ar fi conturat exterior un corp, el urmează forţa de gravitaţie.
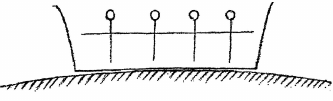
Dacă acţionăm asupra unui număr de corpuri solide luând suportul de sub ele, constatăm că toate cad pe Pământ după linii paralele. Această cădere o putem prezenta în modul următor: Am putea spune, că indiferent de forma pe care o au corpurile solide, ele cad pe Pământ după o perpendiculară pe suprafaţa acestuia (Fig. 6.2). Dacă pe de altă parte ducem o perpendiculară pe aceste linii paralele între ele, obţinem o suprafaţă paralelă cu suprafaţa Pământului. Putem lua la un loc toate liniile de gravitaţie perpendiculare pe care le obţinem de la orice corp, încât să putem trasa o suprafaţă comună, paralelă cu suprafaţa Pământului şi perpendiculară pe liniile de gravitaţie. Această suprafaţă rezultă la început printr-un act de gândire. Să ne întrebăm: Unde există în realitate această suprafaţă? Ea este o realitate la corpurile lichide [Nota 27]. La un lichid, pe care-l iau şi-l pun într-un vas, pot vedea, cum ceea ce altminteri eu trasez ca o perpendiculară pe liniile individuale de gravitaţie există în mod real, ca suprafaţă de nivel a lichidului.
Cum este acest lucru şi ce înseamnă el de fapt? Tot ceea ce am prezentat noi acum reprezintă ceva, ce are o imensă impor tanţă. Căci gândiţi-vă că cineva, pentru a vă explica cum este cu suprafaţa de nivel al lichidului, v-ar spune: Acesta este un vas, în interiorul căruia am un lichid ce formează o suprafaţă de nivel. Fiecare particulă de lichid are tendinţa de a cădea pe Pământ. Prin faptul că forţele pe care le conţine lichidul însuşi se opun ca particulele să cadă pe Pământ, se formează suprafaţa de nivel. Aceasta este realitatea. Lichidul face să ia naştere aceasta.
Dacă luaţi poziţia iniţială a corpurilor solide pe care le lăsaţi să cadă, natura însăşi trasează ceea ce dumneavoastră aţi trasat aici în vederea explicaţiei de mai înainte. Iar dumneavoastră trebuie să vă gândiţi pe deasupra şi la suprafaţa de nivel. De aceea eu am spus mai înainte, că la corpurile solide suprafaţa de nivel este gândită iniţial ca o perpendiculară pe linia de gravitaţie. Dacă reflectaţi consecvent asupra acestor lucruri, veţi găsi faptul curios, că ceea ce dumneavoastră faceţi de obicei pentru a aduce gândurile în legătură cu lichidul, aceasta o face un număr de corpuri solide. Acestea vă schiţează oarecum ceea ce la fluid există în mod material. Putem spune: Corpul cu starea de agregare inferioară, corpul solid ne revelează în comportarea lui pe suprafaţa Pământului, ca într-o imagine, ceea ce de fapt există la lichid, ceea ce există material la lichid şi se opune înfăptuirii acestei linii gravitaţionale. Acest lucru devine evident, atunci când eu privesc corpul solid în întreaga lui relaţie cu Pământul.
Gândiţi-vă ce realizez prin aceasta. Dacă eu îmi desenez liniile de gravitaţie şi suprafaţa de nivel sub impresia căderii unui sistem de corpuri solide, prin aceasta aş obţine o imagine a acţiunii forţei de gravitaţie. Aceasta ar fi în mod direct o imagine a materiei în stare lichidă.
Acum putem merge mai departe. Dacă lăsăm apa la o anumită temperatură suficient de mult timp (într-un vas) – de aceea spuneam eu, că toate lucrurile sunt relative [Nota 28] –, ea dispare de acolo. Apa se evaporă întotdeauna într-un fel sau altul, ceea ce însemnă că de fapt există numai o stare relativă, pentru care putem spune că ea formează o suprafaţă de nivel; pentru a avea o formă, apa trebuie să fie susţinută însă din celelalte laturi, în timp ce dinspre o latură formează o suprafaţă de nivel. – Ea se evaporă neîncetat, iar în vacuum mai repede. De aceea am putea să spunem, că dacă desenăm aici nişte linii, după care apa tinde de fapt continuu, atunci acestea trebuie să fie liniile de forţă ale apei, linii după care ea se şi evaporă realmente. Dar dacă desenăm aceste linii după care tinde apa, nu obţin altceva decât imaginea unui gaz, ce se află într-un spaţiu închis din toate părţile şi care tinde să se pulverizeze în toate direcţiile.
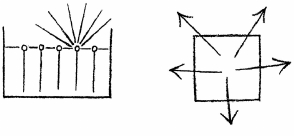
La suprafaţa apei există o tendinţă în acest sens, care – o desenez pentru a o explica – este o imagine a ceea ce se petrece într-adevăr, atunci când las liber un gaz şi el se răspândeşte în toate direcţiile. Astfel că eu pot din nou să spun: Ceea ce remarc drept forţă la lichid, reprezintă o imagine a ceea ce la gaz este o realitate materială.
Avem un fapt curios: Dacă privim într-un mod corect lichidele, percepem la ele imagini ale stării gazoase. Dacă privim într-un mod corect corpurile solide, percepem la ele imagini ale stării
lichide. În fiecare stare de agregare inferioară apar imagini ale stării imediat superioare. Să extindem aceasta până sus. Putem spune: La corpurile solide descoperim imagini ale stării lichide.
La corpurile lichide descoperim imagini ale stării gazoase. La corpurile gazoase descoperim imagini ale căldurii. Ne vom ocupa de aceasta în mod special mâine. Însă eu vreau să mai adaug ceva:
Am încercat astăzi să găsim – prin gândire – trecerea de la gaze la căldură. Mâine, acest lucru va deveni deja mai clar. Şi dacă urmărim acest parcurs mental:
în solid imagini ale lichidului
în lichid imagini ale gazosului
în gazos imagini ale căldurii,
atunci am făcut deja un pas important. Am dobândit posibilitatea, ca pe baza imaginilor ce ne rezultă din observarea stării gazoase, să avem apoi, în câmpul de observaţie omenesc, manifestări
ale căldurii, şi anume ale fiinţei adevărate a căldurii. Dobândim posibilitatea să lămurim ceva – despre care iniţial trebuia să spunem că ne este necunoscut –, prin faptul că îi căutăm în mod
corect imaginile în cadrul stării gazoase. Imaginile fiinţei căldurii trebuie să le căutăm la corpurile stării gazoase. Fireşte, că trebuie să facem acest lucru în mod corect. Dacă
descriem ansamblul de fenomene deja studiate în maniera în care o face fizica actuală atunci când vorbeşte despre gaze, nu ajungem la nimic. Dar dacă luăm în mod corect în
considerare ceea ce ne-a rezultat pentru stările de agregare sub influenţa presiunii şi temperaturii, atunci vom vedea că ajun gem realmente la constatarea, că gazul ne poate revela ceea ce este
de fapt fiinţa căldurii.
Dar fiinţa căldurii acţionează în continuare şi la răcirea în stările lichidă şi solidă. Şi vom fi nevoiţi să urmărim fiinţa căldurii şi la stările lichidă şi solidă – la starea gazoasă putem vedea aceasta în modul cel mai intuitiv; va trebui să vedem dacă fiinţa căldurii suferă vreo modificare specială la stările lichidă şi solidă, pentru ca apoi, prin compararea cu modul în care ea se manifestă în cadrul stării gazoase, unde ea ne arată cel mai bine imaginile ei, să ajungem la însăşi fiinţa reală a căldurii.